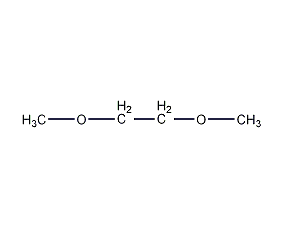
结构式
| 物竞编号 | 031W |
|---|---|
| 分子式 | C4H10O2 |
| 分子量 | 90.12 |
| 标签 |
乙二醇二甲醚, 1,2-二甲氧基代乙烷, 1,2-二甲氧基已烷, 1,2-二甲基乙烷, 乙二醇二甲基醚, 1,2-Ethanediol dimethyl ether, Dimethylglycol, Ethylene glycol dimethyl ether, Monoglyme, 脱漆剂, 稀释剂, 醚和缩醛类溶剂 |
编号系统
CAS号:110-71-4
MDL号:MFCD00008502
EINECS号:203-794-9
RTECS号:KI1451000
BRN号:1209237
PubChem号:24855712
物性数据
1.性状:无色液体,略有醚味。[1]
2.熔点(℃):-58[2]
3.沸点(℃):82~83[3]
4.相对密度(水=1):0.87(20℃)[4]
5.相对蒸气密度(空气=1):3.11[5]
6.饱和蒸气压(kPa):6.40(20℃)[6]
7.燃烧热(kJ/mol):-2521.2[7]
8.临界温度(℃):263[8]
9.临界压力(MPa):3.87[9]
10.辛醇/水分配系数:-0.21[10]
11.闪点(℃):-2(CC)[11]
12.引燃温度(℃):202[12]
13.爆炸上限(%):18.7[13]
14.爆炸下限(%):1.9[14]
15.溶解性:溶于水,溶于乙醇、烃类。[15]
16.折射率(n20ºC):1.3796
17.黏度(mPa·s,20ºC):1.1
18.蒸发热(KJ/mol):28.14
19.熔化热(KJ/kg):139.4
20.生成热(KJ/mol):491.95
21.燃烧热(KJ/mol):2520.82
22.比热容(KJ/(kg·K),定压):1.83
23.电导率(S/m,25ºC):0.47×10-7
24.蒸气压(kPa,20ºC):6.40
25.相对密度(20℃,4℃):0.8665
26.相对密度(25℃,4℃):0.855630
27.临界密度(g·cm-3):0.293
28.临界体积(cm3·mol-1):308
29.临界压缩因子:0.269
30.偏心因子:0.346
31.溶度参数(J·cm-3)0.5:17.732
32.van der Waals面积(cm2·mol-1):8.140×109
33.van der Waals体积(cm3·mol-1):55.200
34.气相标准燃烧热(焓)(kJ·mol-1):-2662.95
35.气相标准声称热(焓)( kJ·mol-1) :-340.24
36.液相标准燃烧热(焓)(kJ·mol-1):-2626.65
37.液相标准声称热(焓)( kJ·mol-1):-376.64
38.液相标准热熔(J·mol-1·K-1):186.5
毒理学数据
1、急性毒性:小鼠经口LC50:3200mg/kg;大鼠经口LD50:>5000mg/kg;兔子经口LD50:320mg/kg;大鼠经口LDL0:1000mg/kg;大鼠皮肤LD50:5370mg/kg;兔子皮肤LDL0:2000mg/kg;大鼠吸入LDL0:63mg/m3/6H
2、吸入和经口属低毒类。吸入高浓度蒸气时,对肺、肝、肾等器官都有损害。
3.急性毒性[16] LD50:775mg/kg(大鼠经口)
生态学数据
该物质对水体有轻微的危害,不要让该产品接触地下水、水道或者污水系统。
分子结构数据
1、摩尔折射率:24.07
2、摩尔体积(cm3/mol):1107.2
3、等张比容(90.2K):230.6
4、表面张力(dyne/cm):21.3
5、极化率(10-24cm3):9.54
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:2
4.可旋转化学键数量:3
5.互变异构体数量:无
6.拓扑分子极性表面积18.5
7.重原子数量:6
8.表面电荷:0
9.复杂度:17.5
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.化学性质:性质稳定,不易发生反应。但能与碘化氢、溴化氢、浓反应。酸性催化剂存在时,高温能发生分解。在150℃以下对碱金属稳定,金属钠可用乙二醇二烷基醚干燥。但能与钠钾合金或钾反应。基锂、丁基锂使乙二醇二甲醚稍有分解。与活性小的Grignard试剂如甲基氯化镁在通常条件下不发生反应,但加热到150~200℃时与活性大的试剂如甲基碘化镁作用而分解。对碱金属的氢化物稳定,可作氢化铝锂的稳定剂、精制剂。在氧的作用下生成过氧化物,光和热对过氧化物的生成有促进作用。生成的过氧化物不稳定,分解成醛、酮、酸及其他杂质。
2.稳定性[17] 稳定
3.禁配物[18] 强氧化剂、强酸
4.避免接触的条件[19] 空气、光照
5.聚合危害[20] 不聚合
贮存方法
储存注意事项[21] 通常商品加有稳定剂。储存于阴凉、通风的库房。远离火种、热源。库温不宜超过37℃,包装要求密封,不可与空气接触。应与氧化剂、酸类分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。
合成方法
1.由乙二醇单甲醚与金属钠;氯甲烷反应而得。将乙二醇单甲醚与金属钠一起回流,直至金属钠完全反应,降温至45℃,通入氯甲烷。反应毕,进行分馏,收集84-85.5℃馏分,即得成品。
精制方法:过氧化物的检验方法与相同。过氧化物可用氯化亚锡一起回流或通过活性氧化铝除去。然后添加少量的金属钠以除微量的水分。其他精制方法有先用钠丝干燥,在氮气流下加氢化铝锂蒸馏。也可以先用无水氯化钙干燥数天,过滤、加金属钠蒸馏,或加氢化铝锂保存,用前蒸馏。
2.边搅拌边将金属钠于60℃下分次少量加到乙二醇单甲醚中,控制温度在78~81℃,金属钠加完后,降温至45℃,然后通入氯甲烷。反应式为:

反应结束后,蒸馏,收集84.5~85.5℃馏分,即得乙二醇二甲醚。
3.用钠丝干燥后,在氮气存在下加氢化铝锂蒸馏,也可用无水氯化钙干燥数天后,滤去氯化钙,再加金属钠蒸馏,或加入氢化铝锂后放置,现用现蒸馏。
用途
1.用作硝酸纤维素、树脂等的溶剂以及制备碱金属氧化物、硼烷时的溶剂。萘、联、三联、蒽等芳香烃在乙二醇二甲醚中与钠生成络合物。钠-萘络合物在聚四氟乙烯等含氟树脂黏合时用于表面处理。钠-联络合物用于汽油中的卤素测定。还可用于从稀水溶液中回收。也用于脱漆剂、稀释剂及增加润滑油的黏度等。
2.用作溶剂、医药抽提剂、有机合成中间体、催化剂、腐蚀抑制剂。[22]




